Brasil
Anvisa aprova uso de remdesivir contra covid-19 e diz que remédio reduz tempo de hospitalização
Medicamento pode ser usado em pacientes hospitalizados acima de 12 anos com necessidade de oxigênio, mas que não estejam intubados. Valor do tratamento ainda é alto, o que dificulta sua utilização pelo SUS
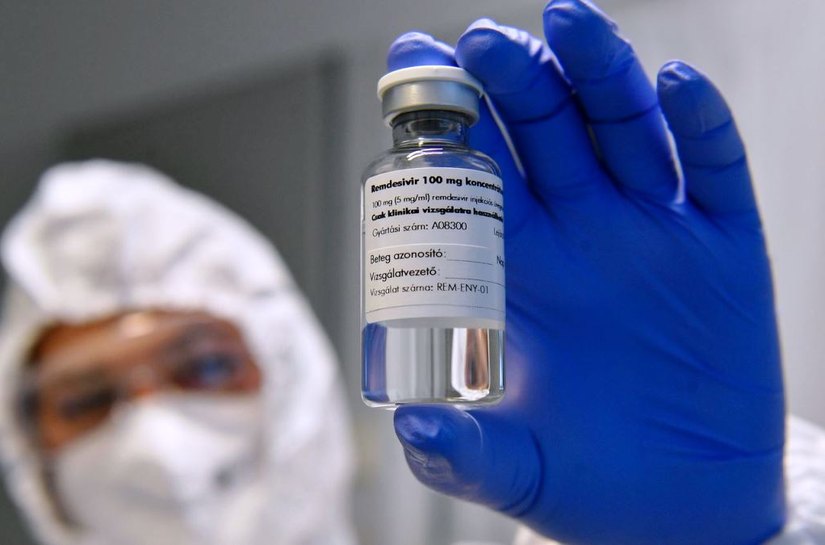
Ao menos 50 países já aprovaram o uso do remdesivir para auxiliar no tratamento da covid-19. O medicamento foi aprovado para uso emergencial nos Estados Unidos em maio do ano passado ―inclusive usado no tratamento do ex-presidente Donald Trump― e também é autorizado em países da Europa. Embora seja um antiviral, não há dados científicos que comprovem a capacidade dele em reduzir a carga viral dos pacientes. Por isso, devem ser considerados os quadros clínicos individuais. “Esta questão [da redução da carga viral] vai ser avaliada em outro momento posterior”, explica Soares. Não deve ser usado, por exemplo, para prevenir a covid-19. A expectativa é que o medicamento possa ajudar a desafogar o sistema de saúde brasileiro, quando o ritmo de vacinação ―única alternativa para diminuir a possibilidade de contrair a doença― ainda é lento.
Por enquanto, não há perspectiva clara de que o remdesivir poderá ser incorporado rapidamente ao SUS em escala. Trata-se de um medicamento caro, cujo tratamento custa em média 3.120 dólares (cerca de 17.000 reais). Uma câmara de medicamentos composta por vários ministérios, como o da Saúde e o da Economia, e secretariada pela Anvisa ainda precisa definir o teto do valor do medicamento. No Brasil, apenas a empresa Gilead, detentora da patente que solicitou o registro à agência, pode comercializá-lo. “Este é um procedimento à parte que agora vai ser deliberado”, diz Gustavo Mendes. Ele aponta que, sem a definição do teto, é difícil disponibilizar o produto. O EL PAÍS procurou o Ministério da Saúde para comentar a questão, mas ainda não houve resposta.
Questionado sobre o porquê de a Anvisa ter tomado esta decisão neste momento ―já que a agência o analisava desde meados do ano passado e outros países haviam autorizado o uso, os técnicos apontaram que o mecanismo de autorização emergencial não estava previsto no Brasil e que eles consideraram os dados ainda insuficientes para um registro condicional, que permite o acréscimo de novas informações posteriormente mediante a assinatura de termos de compromisso. “O registro pode ser dado de maneira condicional, mas o comitê entendeu que era preciso ter mais dados para tomar esta decisão”, afirma Mendes.
Vacina da AstraZeneca tem registro definitivo
A Anvisa também concedeu o registro definitivo à AstraZeneca e à Fiocruz para sua vacina contra a covid-19. O imunizante, já em uso no país, tinha apenas o registro emergencial. Com a decisão, está permitido o uso em larga escala, a entrega de doses finalizadas pela Fiocruz e se abre também espaço para a comercialização. Isso porque o registro foi concedido tanto para a Fiocruz ―que negocia apenas com o Governo e organismos internacionais― quanto para a farmacêutica AstraZeneca. “Abre a prerrogativa para uma comercialização, e isso vai ser definido pelas próprias empresas”, aponta Mendes.
Nesta semana, a vacina da AstraZeneca foi suspensa temporariamente e por precaução em cinco países (Romênia, Tailândia, Bulgária, Dinamarca e Finlândia) depois que algumas pessoas, que haviam tomado essas doses, desenvolveram coágulos sanguíneos. Não há, entretanto, um aumento significativo de casos e nem uma correlação estabelecida. A Anvisa ―que seguirá acompanhando possíveis efeitos adversos mesmo após o registro, assim como dados de eficácia para grupos específicos― explicou que os casos observados nestes países estavam relacionados a um lote específico que não veio ao país, que até agora distribuiu apenas doses fabricadas no instituto indiano Serum. No Brasil, cinco pessoas de um universo de mais de 2 milhões que receberam a vacina apresentaram efeitos semelhantes, mas a Anvisa diz que não vê relação de causa com o imunizante. Os pacientes, idosos e passíveis de AVC e trombose, seguem sendo monitorados. A Agência Europeia de Medicamentos, que investiga a relação entre as vacinas e esses efeitos, salienta que não há ainda nenhuma comprovação de ligação entre os casos de trombose nos cinco países mencionados e a vacina.
